 C .
C . 
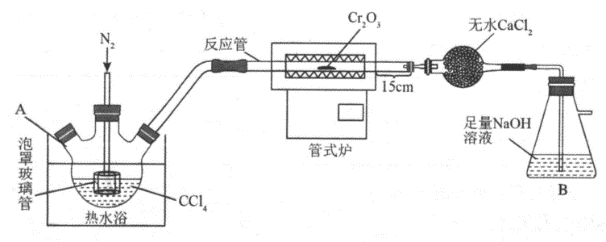
已知:有剧毒,与水反应生成两种酸性气体.
回答下列问题:
a.先停止加热,再停止通入 b.先停止通入
, 再停止加热
称取样品溶于水配制成
溶液,取
所得溶液于锥形瓶中,加入
的
溶液,充分反应后,加入指示剂,用
的
标准溶液滴定至终点时,消耗标准溶液的体积为
(已知:
、
).
该样品中的质量分数为(计算结果精确到
).如果滴定管用蒸馏水洗涤后未用标准溶液润洗,则测定结果(填“偏高”、“偏低”或“无影响”).
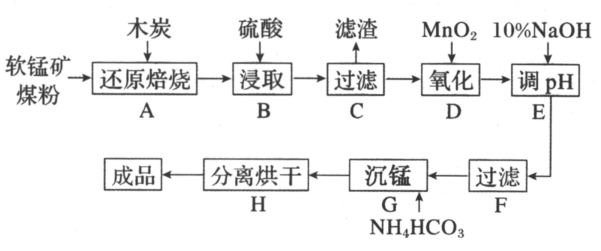
已知:①软锰矿煤粉的主要成分是 , 还含有少量
和
及其氧化物等;
②还原焙烧时被还原成
;
③可能用到的数据如下:
氢氧化物 | ||||
开始沉淀时 | 1.5 | 6.5 | 4.2 | 8.3 |
沉淀完全时 | 3.7 | 9.7 | 7.4 | 9.8 |
回答下列问题:
A. B.
C.
D.
②
③
反应 .
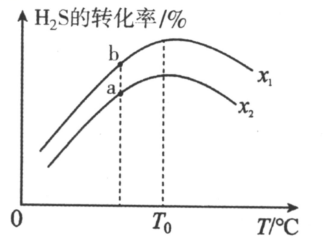
①(填“>”“<”或“=”,下同)
.
①时,在密闭容器中充入等物质的量的
和
发生上述反应,则平衡时
的体积分数为.
②在两个密闭容器中都加入四种气体,起始时气体体积分数
, 分别在
和
时反应,容器中
和
的体积分数
随时间
的变化关系如图所示:
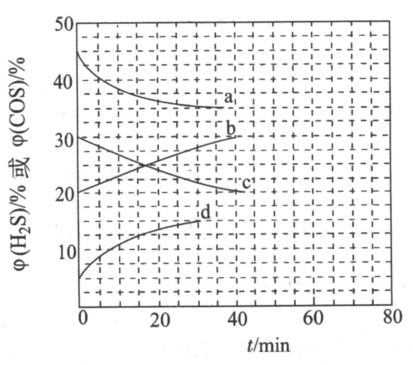
和
时,
随时间变化关系的曲线分别是、,判断的理由是.
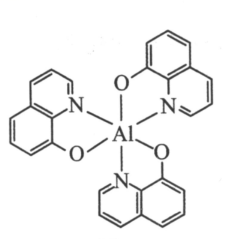
图1
A.共价键 B.离子键 C.配位键 D.氢键
氧化物 | |||
沸点 | 100 |
①表中氧化物之间沸点差异的原因为.
②的VSEPR模型为.
③和
分子中,键角更大的是(填化学式).
若阿伏加德罗常数的值为晶体的密度为
晶体的密度为
, 则
晶体与
晶体的晶胞参数之比为.
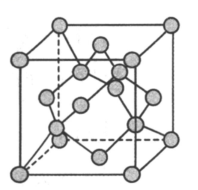
图2